Quy tắc đàng chéo cánh – Phương pháp đàng chéo cánh.
- Phương pháp đàng chéo cánh là cách thức thông thường được vận dụng cho những câu hỏi láo lếu phù hợp chứa chấp 2 bộ phận nhưng mà đòi hỏi của câu hỏi là xác lập tỉ lệ thành phần thân thuộc 2 bộ phận ê.
- Đây là phương pháp có nhiều ưu điểm, giúp tăng tốc độ tính toán, và là 1 công cụ bổ trợ rất đắc lực cho tới phương pháp trung bình.
- Phương pháp đường chéo có thể áp dụng tốt cho tới nhiều trường hợp, nhiều dạng bài tập, đặc biệt là dạng bài trộn chế dung dịch và tính thành phần hỗn hợp.
Thường sử dụng kết hợp giữa đường chéo với phương pháp trung bình và phương pháp bảo toàn vẹn toàn tố. Với hỗn hợp phức tạp có thể sử dụng kết hợp nhiều đường chéo.
Trong nhiều số trường hợp ko cần thiết phải viết sơ đồ dường chéo nhằm rút ngắn thời gian lận làm bài. - Nhược điểm của phương pháp này là ko áp dụng được cho tới những bài toán vô đó có xảy rời khỏi phản ứng giữa các chất tan với nhau, ko áp dụng được với trường hợp tính toán pH
Các bước giải câu hỏi vày cách thức đàng chéo
Bạn đang xem: Quy tắc đường chéo- Phương pháp trung bình
- Xác quyết định trị số cần thiết dò xét kể từ đề bài
- Chuyển những số liệu lịch sự dạng đại lượng % khối lượng
- Xây dựng đàng chéo cánh → Kết ngược câu hỏi.
Các dạng bài xích luyện về cách thức đàng chéo
- Dạng 1: Tính toán dung lượng những đồng vị
+) Đồng vị là những vẹn toàn tử sở hữu nằm trong số proton tuy nhiên không giống nhau về số khối nên nằm trong tuỳ thuộc một nhân tố chất hóa học và sở hữu nằm trong địa điểm vô bảng tuần trả những nhân tố chất hóa học.
+) Khác với số khối của đồng vị, lượng vẹn toàn tử khoảng là độ quý hiếm khoảng những số khối của đồng vị tạo ra nhân tố ê. Trong tình huống nhân tố được tạo ra vày 2 đồng vị hầu hết, tớ hoàn toàn có thể đơn giản tính được dung lượng hóa học từng đồng vị vày cách thức đàng chéo
Ví dụ:

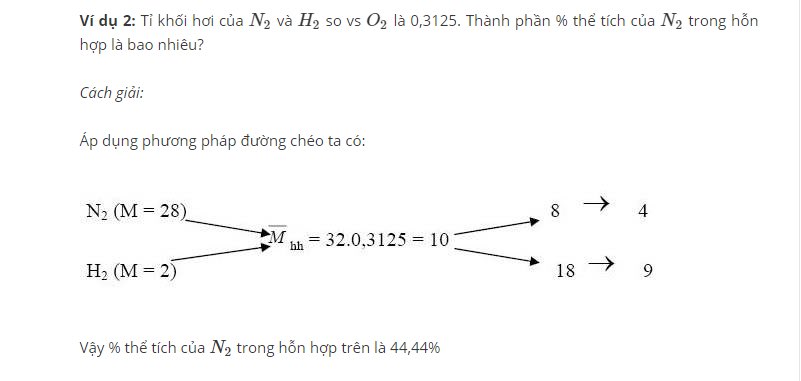
- Dạng 2: Tính tỷ trọng bộ phận của láo lếu phù hợp khí qua chuyện tỷ khối
Ví dụ:
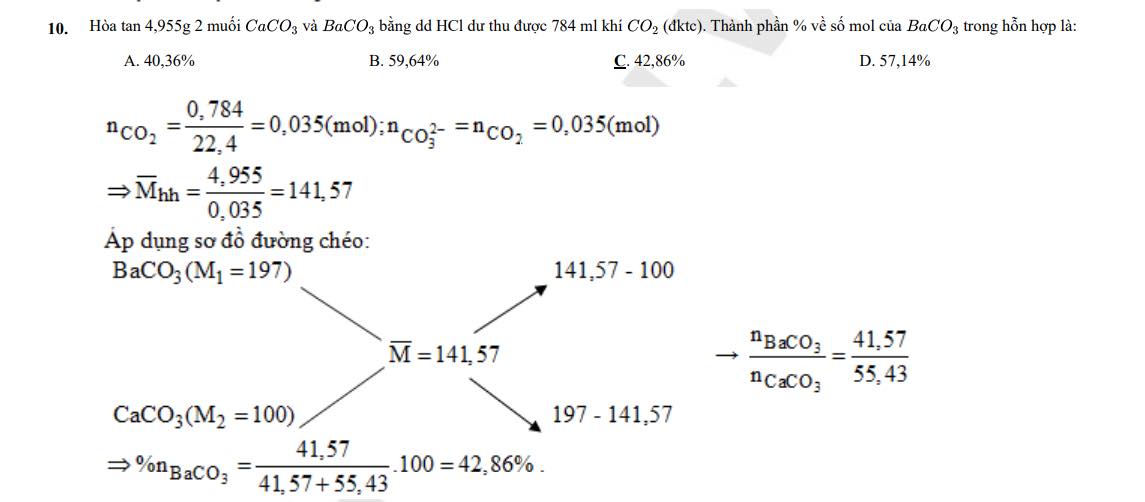
Dạng 3: Tính tỷ trọng những hóa học vô láo lếu phù hợp 2 hóa học vô cơ
Ví dụ:
Dạng 4: Tính tỷ trọng những hóa học vô láo lếu phù hợp nhị hóa học hữu cơ

Xem thêm: Lợi ích sức khỏe từ cải thìa: Ai nên ăn thường xuyên?
Dạng 5: Tính toán vô pha trộn những hỗn hợp sở hữu nằm trong hóa học tan
- Dung dịch 1: Có lượng m1, thể tích V1, độ đậm đặc C1, lượng riêng rẽ d1
- Dung dịch 2: Có lượng mét vuông, thể tích V2, độ đậm đặc C2 (C2>C1), lượng riêng rẽ d2
- Dung dịch thu được: sở hữu lượng m=m1+m2, thể tích V=V1+V2 và lượng riêng rẽ d.
Một số bài xích luyện tự động vận dụng
Bài 1:Hoà tan trọn vẹn 5,2 gam nhị sắt kẽm kim loại kiềm ở nhị chu kì sau đó nhau vô nước chiếm được 2,24 lít H2 (đktc) cất cánh rời khỏi. Hai sắt kẽm kim loại ê là:
A. Li và Na B. Na và K C. K và Rb D. Rb và Cs
Bài 2:Hỗn phù hợp A bao gồm 2 sắt kẽm kim loại X,Y sở hữu hóa trị ko thay đổi và không tồn tại sắt kẽm kim loại này hóa trị I. Lấy 7,68g láo lếu phù hợp A tạo thành 2 phần vày nhau:
– Phần 1: nung vô khí O2 dư nhằm lão hóa trọn vẹn, chiếm được 6g láo lếu phù hợp rắn B bao gồm 2 oxit
– Phần 2: hòa tan trọn vẹn vô dd chứa chấp HCl và H2SO4 loãng, chiếm được V lit khí H2 (đktc) và ddC. Tính V.
A. 2,352 lit B. 4,704 lit C. 3,024 lit D. 1,176 lit
Bài 3: Cho 14 gam láo lếu phù hợp nhị anken là đồng đẳng tiếp tục trải qua hỗn hợp nước Br2 thấy làm mất đi color một vừa hai phải đầy đủ hỗn hợp chứa chấp 64 gam Br2 . Công thức phân tử của những anken là
A. C2H4; C3H6 B. C3H6; C4H8 C. C4H8; C5H10 D. C5H10; C6H12
Bài 4: Cho axit oxalic HOOC-COOH tính năng với láo lếu phù hợp nhị ancol no, đơn chức, đồng đẳng tiếp tục chiếm được 5,28 gam láo lếu phù hợp 3 este trung tính. Thủyphân lượng este bên trên vày hỗn hợp NaOH chiếm được 5,36 gam muối bột. Hai rượu sở hữu công thức:
A. CH3OH; C2H5OH B. C2H5OH; C3H7OH C. C3H7OH; C4H9OH D.C4H9OH; C5H11OH
Xem thêm: TPCN hỗ trợ sinh lý nam
Xem thêm:
Phương trình ion rút gọn gàng – Dạng bài xích luyện thông thường gặp gỡ vô đề thi
Định luật bảo toàn năng lượng điện – Dạng bài xích luyện thông thường gặp gỡ vô đề thi











Bình luận