Bảng tuần trả các nguyên tố chất hóa học là bảng bao quát cộng đồng nhất về cấu trúc nguyên vẹn tử của những thành phần bên trên ngược khu đất. Đây là phần học tập vô nằm trong cần thiết nhập kỹ năng Hóa học tập 10, nhằm làm rõ rộng lớn về phần học tập này, hãy nằm trong VUIHOC dò la hiểu về lý thuyết và thực hiện một trong những bài xích tập dượt ôn luyện nhé!
1. Sơ lược cộng đồng về bảng tuần trả các nguyên tố hoá học
Bảng tuần trả các nguyên tố chất hóa học biên soạn nhập năm 1869 bởi vì căn nhà chất hóa học người Nga – Dimitri Mendeleev. Bảng tuần trả các nguyên tố chất hóa học chung người học tập dễ dàng và đơn giản bố trí, nhận ra và thâu tóm đúng chuẩn quy luật của các nguyên tố chất hóa học nhập bảng.
Bạn đang xem: Cách đọc bảng tuần hoàn các nguyên tố hoá học dễ hiểu nhất - VUIHOC
Khi các nguyên tố vừa được nhìn thấy, bảng tuần trả các nguyên tố hoá học tập vẫn nên trải qua chuyện thật nhiều phen kiểm soát và điều chỉnh. Tuy nhưng, những kiểu dáng hiển thị cơ bạn dạng vẫn không thay đổi như design ban sơ của Mendeleev.
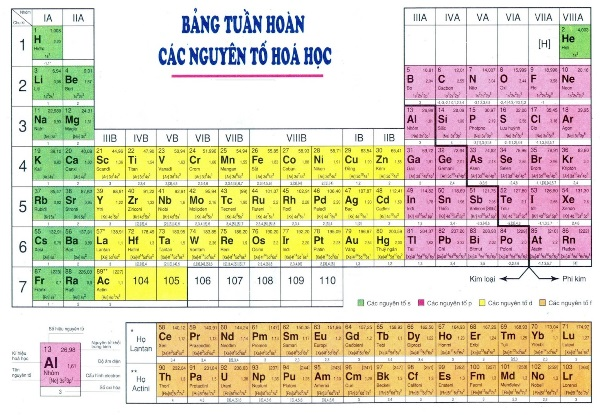
2. Cấu tạo ra nhập bảng tuần trả các nguyên tố hoá học
2.1. Ô thành phần nhập bảng tuần trả các nguyên tố hoá học
Thể hiện nay được những vấn đề về: số hiệu nguyên vẹn tử, ký hiệu chất hóa học, tên thường gọi của thành phần, nguyên vẹn tử khối của thành phần chất hóa học trong những dù.
2.2. Chu kỳ
Dãy các nguyên tố chất hóa học sẽ tiến hành bố trí theo hướng tăng dần dần năng lượng điện phân tử nhân và những nguyên vẹn tử của các nguyên tố bại liệt đem nằm trong số lớp electron. Có tổng toàn bộ 7 chu kỳ luân hồi nằm trong bảng tuần trả các nguyên tố chất hóa học. Chu kỳ 1, 2, 3 gọi là chu kỳ luân hồi nhỏ và chu kì 4, 5, 6, 7 gọi là chu kỳ luân hồi rộng lớn.
2.3. Nhóm nguyên vẹn tố
Tập ăn ý các nguyên tố đem đặc điểm tương tự động nhau bởi nhập nguyên vẹn tử của bọn chúng đem nằm trong số electron phần bên ngoài nằm trong và được xếp trở nên cột theo hướng tăng dần dần năng lượng điện phân tử nhân kể từ bên dưới tăng trưởng bên trên.
Có 2 group thành phần đó là group A và group B:
– Các thành phần A nhập bảng tuần trả là: bao hàm các nguyên tố s và p. Số trật tự group A bởi vì tổng số electron phần bên ngoài nằm trong.
– Các thành phần B nhập bảng tuần trả là: bao hàm các nguyên tố d và f đem thông số kỹ thuật electron nguyên vẹn tử thì tận nằm trong ở dạng (n-1)dxnsy:
+ Nếu (x+y) = 3 → 7 thì thành phần này nằm trong group (x+y)B.
+ Nếu (x+y) = 8 → 10 thì thành phần này nằm trong group VIIIB.
+ Nếu (x+y) > 10 thì thành phần này nằm trong group (x+y-10)B
3. Số lượng thành phần nhập bảng tuần trả các nguyên tố hoá học
Tính đến giờ, đem tổng số đem 118 thành phần nhập bảng tuần trả các nguyên tố chất hóa học đang được xác thực, bao hàm kể từ thành phần 1 (Hydro) cho đến thành phần 118 Oganesson.
Trong tổng số 118 thành phần nhập bảng thì đem tới 98 thành phần xuất hiện nay ở nhập ngẫu nhiên, đôi mươi thành phần sót lại kể từ thông thường chỉ xuất hiện nay ở dạng tổ hợp tự tạo.
Trong số 98 thành phần đem nhập ngẫu nhiên thì có tầm khoảng 84 thành phần là nguyên vẹn thuỷ bọn chúng đang được xuất hiện nay trước lúc Trái khu đất được tạo hình. Khoảng 14 thành phần không nhiều bắt gặp sót lại thông thường chỉ xuất hiện nay ở trong mỗi chuỗi phản xạ phân tan của 84 thành phần nguyên vẹn thuỷ bên trên.
Đăng ký ngay lập tức sẽ được những thầy cô ôn tập dượt và thiết kế trong suốt lộ trình học tập tập THPT vững vàng vàng

4. Cách coi bảng tuần trả thành phần hoá học
Dưới phía trên tất cả chúng ta tiếp tục dò la hiểu về kiểu cách hiểu bảng tuần trả các nguyên tố chất hóa học một cơ hội thiệt chi tiết:
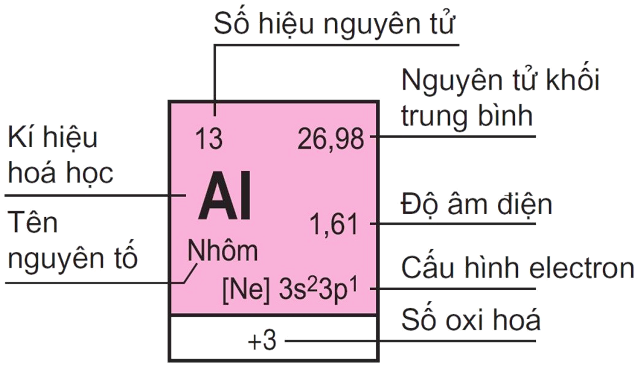
4.1. Số nguyên vẹn tử
Có tên thường gọi không giống là số proton của các nguyên tố chất hóa học. Số hiệu nguyên vẹn tử biểu thị mang đến số proton của một nguyên vẹn tử và số năng lượng điện ở nhập phân tử nhân. Số hiệu nguyên vẹn tử có mức giá trị tương tự với số electron đem nhập một nguyên vẹn tử hòa hợp về năng lượng điện. Số hiệu nguyên vẹn tử sẽ hỗ trợ tớ xác lập có một không hai một thành phần chất hóa học.
4.2. Nguyên tử khối trung bình
Hầu không còn các nguyên tố chất hóa học là lếu láo ăn ý của vô vàn những đồng vị với tỷ trọng % số nguyên vẹn tử xác lập. Vậy nên nguyên vẹn tử khối của những thành phần có rất nhiều đồng vị thông thường được xem là nguyên vẹn tử khối khoảng của lếu láo ăn ý đồng vị và tính cho tới tỷ trọng xác suất của số nguyên vẹn tử ứng.
4.3. Độ âm điện
Là tài năng bú mớm electron nhập quy trình tạo hình links chất hóa học. Độ âm năng lượng điện tiếp tục tỉ trọng thuận với tính phi kim. Nếu phỏng âm năng lượng điện của thành phần càng rộng lớn thì tính phi kim càng mạnh và ngược lại.
4.4. Cấu hình electron
Cho thấy được sự phân bổ của những electron trong mỗi tình trạng tích điện không giống nhau ở lớp vỏ nguyên vẹn tử hoặc ở những điểm tuy nhiên bọn chúng xuất hiện.
4.5. Số oxi hoá
Là số được dùng cho một hoặc 1 group những nguyên vẹn tử. Nhờ nhập số lượng này, tất cả chúng ta rất có thể tính được số electron trao thay đổi Lúc bọn chúng nhập cuộc phản xạ.
4.6. Tên nguyên vẹn tố
Gồm 1 loại nguyên vẹn tử có một không hai và được phân biệt phụ thuộc vào số hiệu nguyên vẹn tử.
4.7. Ký hiệu hoá học
Là thương hiệu ghi chép tắt của từng thành phần chất hóa học, gồm một cho tới 2 vần âm Latin. Chữ trước tiên của các nguyên tố thông thường tiếp tục ghi chép hoa.
5. Mẹo học tập nằm trong thời gian nhanh bảng tuần trả các nguyên tố hoá học
5.1. Học bảng tuần trả trải qua cơ hội học tập truyền thống
Trong cách thức này, rất cần phải nhận ra được những bộ phận thành phần bám theo 7 mục tuy nhiên một vừa hai phải liệt kê phía trên. Theo bại liệt, thường ngày, những em nên chia nhỏ ra học tập kể từ 3-5 thành phần nhằm dễ dàng ghi lưu giữ rộng lớn và ghi lưu giữ lâu lâu năm.
Để thuận tiện mang đến việc học tập rộng lớn, những em rất có thể dán bảng tuần trả ở từng những chống dễ thương hoặc hoặc trải qua. Khi bại liệt, những em rất có thể bắt gặp và dễ dàng và đơn giản hiểu với những thành phần bại liệt trong thời gian ngày.
5.2. Sử dụng những bài xích vè, bài xích thơ tương hỗ lưu giữ nhanh
Việc đem những sản phẩm thành phần chất hóa học sang trọng những bài xích văn hoặc bài xích thơ sẽ hỗ trợ tài năng học tập nằm trong của những em trở thành dễ dàng và đơn giản rộng lớn.
Mẹo 1: Học nằm trong lời nói sướng mang đến 16 thành phần hoạt động và sinh hoạt hoá học tập của thành phần kim loại:
“ Khi này cần thiết may áo giáp Fe nên sang trọng phố chất vấn cửa hàng Á Phi Âu “ ứng l với các nguyên tố theo lần lượt là: K, Na, Ca, Mg, Al, Zn, Fe, N, S, P.., H, Cu, Hg, Ag, Pt, Au.
Mẹo 2: Học nằm trong 6 thành phần group IA qua chuyện câu nói:
“Lâu ni ko rảnh coi phim” ứng với các nguyên tố theo lần lượt là Li, Na, K, Rb, Cs, Pr
5.3. Nghiên cứu vãn và ghi lưu giữ quy luật của bảng tuần hoàn
Mỗi dù nhập bảng tuần trả các nguyên tố chất hóa học tiếp tục hiển thị vấn đề về thương hiệu, ký hiệu và số hiệu nguyên vẹn tử của thành phần. Chỉ cần thiết ghi lưu giữ khoảng chừng 10 thành phần trước tiên, những em rất có thể dò la rời khỏi được những quy luật mang đến các nguyên tố sót lại.
5.4. In và dán bảng tuần trả ở những điểm dễ dàng nhận biết nhập không khí học
Các em hãy dán bảng tuần trả ở những điểm dễ dàng để ý, hoặc nhằm ý nhất rồi tạo thành nhiều phần nhằm dễ dàng học tập. Vấn đề này thiệt sự mang tới hiệu suất cao rất rất cao trong những công việc ghi lưu giữ kỹ năng cộng đồng.
6. Bài tập dượt áp dụng bảng tuần trả các nguyên tố hoá học
6.1. Bài tập dượt tự động luận cơ bạn dạng và nâng lên SGK
Ví dụ 1: Nhìn nhập group VIIIB nhập bảng tuần trả, mang đến ghi chép group này còn có điểm sáng gì khác lạ đối với những group còn lại
Lời giải:
Nhóm VIIIB sẽ sở hữu được 3 cột còn những group không giống chỉ có một cột.
Các thành phần nằm trong group VIIIB ở nhập bảng tuần trả sẽ sở hữu được tổng số electron phần bên ngoài nằm trong và ngay gần phần bên ngoài nằm trong ko bão hòa (electron hóa trị) tiếp tục cân nhau.
Ví dụ 2: Dựa nhập thông số kỹ thuật electron, cho biết thêm thành phần đem số hiệu thành phần là 6, 8, 18, đôi mươi nằm trong khối thành phần này nhập bảng tuần trả. Các thành phần này là sắt kẽm kim loại, phi kim hay những khí khan hiếm.
Lời giải:
Nguyên tố đem số hiệu nguyên vẹn tử bởi vì 6 đem thông số kỹ thuật electron là: 1s22s22p4
⇒ Thuộc khối thành phần group p, là thành phần phi kim.
Nguyên tố đem số hiệu nguyên vẹn tử bởi vì 8 đem thông số kỹ thuật electron là: 1s22s22p63s23p6
⇒ Thuộc khối thành phần group p, là thành phần phi kim.
Nguyên tố đem số hiệu nguyên vẹn tử bởi vì 18 đem thông số kỹ thuật electron nguyên vẹn tử là: 1s22s22p63s23p6
⇒ Nguyên tố là khí khan hiếm, nằm trong khối thành phần group p.
Nguyên tố đem số hiệu nguyên vẹn tử bởi vì đôi mươi đem thông số kỹ thuật electron nguyên vẹn tử là: 1s22s22p63s23p64s2
⇒ Thuộc khối thành phần group s, là thành phần sắt kẽm kim loại.
Ví dụ 3: Dựa nhập thông số kỹ thuật electron thành phần, hãy cho biết thêm thành phần đem số hiệu nguyên vẹn tử bởi vì đôi mươi nằm trong chu kì này nhập bảng tuần trả các nguyên tố hóa học?
Lời giải:
Cấu hình electron nguyên vẹn tử của thành phần đem Z = đôi mươi là: 1s22s22p63s23p64s2
⇒ Số trật tự chu kì tiếp tục ứng với số lớp electron = 4.
Ví dụ 4: Cho biết số electron phần bên ngoài nằm trong, số proton của nguyên vẹn tử Al.
Lời giải:
Dựa nhập thông số kỹ thuật electron, nguyên vẹn tử aluminium đem 3 electron phần bên ngoài nằm trong, số proton thông qua số electron và bởi vì 13.
Hoặc số proton tiếp tục ứng số hiệu nguyên vẹn tử = 13.
Ví dụ 5: Mô mô tả bảng tuần trả các nguyên tố chất hóa học của Mendeleev. Nhận xét gì về kiểu cách bố trí các nguyên tố chất hóa học bám theo khunh hướng kể từ bên trên xuống bên dưới ở nhập và một cột.
Lời giải:
Bảng tuần trả các nguyên tố chất hóa học bám theo Mendeleev bao gồm những kí hiệu của các nguyên tố chất hóa học và lượng nguyên vẹn tử của những thành phần bại liệt.
Các thành phần này được bố trí nhập những sản phẩm và những cột ứng theo hướng tăng dần dần về lượng nguyên vẹn tử, chính thức nhập sản phẩm mới nhất Lúc đặc điểm của thành phần này bại liệt tái diễn.
6.2. Bài tập dượt trắc nghiệm bảng tuần trả các nguyên tố hoá học
Câu 1: Ở nhập bảng tuần trả các nguyên tố chất hóa học được bố trí bám theo phương pháp nào?
A. Theo chiều tăng của năng lượng điện phân tử nhân nguyên vẹn tử.
B. Các thành phần đem nằm trong số lớp electron nguyên vẹn tử sẽ tiến hành bố trí trở nên 1 sản phẩm.
C. Các thành phần đem nằm trong số electron hoá trị nguyên vẹn tử sẽ tiến hành bố trí trở nên 1 cột.
D. Cả A, B, C.
Câu 2: Chu kì là:
A. Dãy các nguyên tố tuy nhiên nguyên vẹn tử của các nguyên tố bại liệt đem nằm trong số lớp electron và được bố trí theo hướng tăng dần dần lượng nguyên vẹn tử.
Xem thêm: Sinh năm 1995 mệnh gì? Hợp màu gì? Đá phong thủy nào?
B. Dãy các nguyên tố tuy nhiên nguyên vẹn tử của của các nguyên tố đem nằm trong số lớp electron và được xếp theo hướng tăng dần dần số khối.
C. Dãy các nguyên tố tuy nhiên nguyên vẹn tử của các nguyên tố bại liệt đem nằm trong số lớp electron và được xếp theo hướng tăng dần dần năng lượng điện phân tử nhân nguyên vẹn tử.
D. Dãy các nguyên tố tuy nhiên nguyên vẹn tử của các nguyên tố bại liệt đem nằm trong số lớp electron và được xếp theo hướng tăng dần dần số nơtron.
Câu 3: Nhóm thành phần là
A. Tập ăn ý các nguyên tố tuy nhiên nguyên vẹn tử của thành phần này còn có thông số kỹ thuật electron kiểu như nhau và được xếp ở cùng một cột.
B. Tập ăn ý các nguyên tố tuy nhiên nguyên vẹn tử của thành phần này còn có thông số kỹ thuật electron tương tự nhau, vì thế đem đặc điểm hoá học tập kiểu như nhau và được xếp trở nên một cột.
C. Tập ăn ý các nguyên tố tuy nhiên nguyên vẹn tử của thành phần này còn có thông số kỹ thuật electron tương tự động nhau, vì thế đem đặc điểm hoá học tập tương tự nhau và được xếp trở nên một cột.
D. Tập ăn ý các nguyên tố mà nguyên vẹn tử của thành phần này còn có đặc điểm hoá học tập kiểu như nhau và được xếp cùng một cột.
Câu 4: Cho thông số kỹ thuật electron của Mn [Ar]3d54s2. Mn nằm trong thành phần nào?
A. Nguyên tố s B. Nguyên tố p C. Nguyên tố d D. Nguyên tố f
Câu 5: Cho thông số kỹ thuật electron nguyên vẹn tử của Zn: [Ar] 3d104s2. Vị trí của Zn ở nhập bảng tuần trả các nguyên tố chất hóa học là
A. Ô 29, chu kỳ luân hồi 4, group IIA C. Ô 30, chu kỳ luân hồi 4, group IIA
B. Ô 30, chu kỳ luân hồi 4, group IIB. D. Ô 31, chu kỳ luân hồi 4, group IIB.
Câu 6: Oxit tối đa của một thành phần R chứa chấp 38,8% thành phần bại liệt, còn nhập ăn ý hóa học khí với hidro chứa chấp 2,74% hidro. Xác quyết định thành phần R.
A. Cl B. Br C.Ba D. Al
Câu 7: Hợp hóa học của R với thành phần hiđro ở thể khí đem dạng là RH4. Oxit tối đa của thành phần R đem tỉ trọng oxi 53,3% về lượng. Nguyên tố R sẽ sở hữu được số khối là:
A. 12. B. 28. C. 32. D. 31.
Câu 8: Nguyên tố X có hóa trị cao nhất với thành phần oxi bằng với hóa trị nhập hợp chất khí với thành phần hiđro. Phân tử khối của oxit này bằng 2,75 lần phân tử khối của hợp chất khí này với hiđro. Vậy X là nguyên vẹn tố:
A. C. B.Si. C. Ge. D. S.
Câu 9: Nguyên tố X có công thức oxit cao nhất với Oxi là XO2, nhập đó tỉ lệ khối lượng của thành phần X và O là 3/8. Công thức của XO2 tiếp tục là
A. CO2. B. NO2. C. SO2. D. SiO2.
Câu 10: Trong tình trạng cơ bạn dạng, thông số kỹ thuật electron nguyên vẹn tử ở phần bên ngoài nằm trong của nguyên vẹn tử thành phần X là 3s23p1. Vị trí của thành phần X nhập bảng tuần trả tiếp tục là
A. Chu kì 3, group IIIB. B. Chu kì 3, group IA.
C. Chu kì 4, group IB. D. Chu kì 3, group IIIA.
Câu 11: Trong tình trạng cơ bạn dạng, thông số kỹ thuật electron nguyên vẹn tử ở phần bên ngoài nằm trong của nguyên vẹn tử thành phần X là 3s2. Số hiệu nguyên vẹn tử của thành phần X bằng:
A. 12. B. 13. C. 11. D. 14.
Câu 12: Nguyên tử X đem electron ph ởân phần bên ngoài nằm trong là 3p4. Hãy xác lập ý sai trong những ý sau đây Lúc nói đến nguyên vẹn tử X
A. Lớp ngoài nằm trong của nguyên vẹn tử X đem 6 electron
B. Hạt nhân của nguyên vẹn tử X đem 16 electron
C. Trong bảng tuần trả các nguyên tố chất hóa học, thành phần X thuôc chu kì 3
D. Nguyên tố X ở nằm trong group VIA
Câu 13: Nguyên tử R tạo ra Anion R2-. Cấu hình electron nguyen tử của R2- ở tình trạng cơ bạn dạng là 3p6. Tổng số phân tử đem năng lượng điện nhập nguyên vẹn tử R là.
A.18 B.32 C.38 D.19
Câu 14: Nguyên tử của thành phần A đem tổng số electron ở phân lớp p là 5, Vị trí của thành phần A nhập bảng tuần trả là
A. Nhóm VA, chu kì 3. B. VIIA, chu kì 2.
C. VIIB, chu kì 2. D. VIA, chu kì 3.
Câu 15: X là thành phần p. Tổng số phân tử đem nhập nguyên vẹn tử của thành phần X bởi vì 40. Vị trí của thành phần X nhập bảng tuần trả các nguyên tố chất hóa học là
A. Ô loại 40, chu kỳ luân hồi 5, group IVB. B. Ô loại 14, chu kỳ luân hồi 3, group IIA.
C. Ô loại 13, chu kỳ luân hồi 3, group IIIA. D. Ô loại 15, chu kỳ luân hồi 3, group VA.
Câu 16: Nguyên tố X (Z=34). Vị trí của X là
A. Ô loại 34, chu kỳ luân hồi 4, group VIA. B. Ô loại 34, chu kỳ luân hồi 4, group VIB
C. Ô loại 34, chu kỳ luân hồi 4, group VA. D. Ô loại 34, chu kỳ luân hồi 4, group VB.
Câu 17: Nguyên tử của thành phần này sau đây đem khuynh phía tiếp tục nhường nhịn 1 electron ở trong những phản xạ hóa học?
A. Na nằm trong dù loại 11 nhập bảng tuần trả.
B. Mg nằm trong dù loại 12 nhập bảng tuần trả.
C. Al nằm trong dù loại 13 nhập bảng tuần trả.
D. Si ở nằm trong loại 14 nhập bảng tuần trả.
Câu 18: Một thành phần R đem thông số kỹ thuật electron nguyên vẹn tử là: 1s22s22p63s23p4, công thức của ăn ý hóa học thân thiết R với hiđro và công thức oxit tối đa tiếp tục là:
A. RH2, RO. B. RH2, RO3. C. RH2, RO2. D. RH5, R2O5.
Câu 19: Nguyên tố nằm trong số lần 5 và nhóm VIA có cấu hình electron hóa trị tiếp tục là
A. …6s26p6. B. …6s26p3. C. …5s25p6. D. …5s25p4.
Câu 20: Nguyên tố X đem thông số kỹ thuật electron nguyên vẹn tử là 1s22s22p3. Vậy địa điểm của thành phần X nhập bảng tuần trả và công thức của ăn ý hóa học khí với hiđro của thành phần X là :
A. Chu kì 2, group VA, HXO3.
B. Chu kì 2, group VA, XH4.
C. Chu kì 2, group VA, XH3.
D. Chu kì 2, group VA, XH2.
Đáp án tham lam khảo:
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
| D |
C |
C |
C |
B |
A |
B |
A |
A |
D |
| 11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
| A |
B |
B |
B |
C |
A |
A |
B |
B |
C |
PAS VUIHOC – GIẢI PHÁP ÔN LUYỆN CÁ NHÂN HÓA
Khóa học tập online ĐẦU TIÊN VÀ DUY NHẤT:
⭐ Xây dựng trong suốt lộ trình học tập kể từ tổn thất gốc cho tới 27+
⭐ Chọn thầy cô, lớp, môn học tập bám theo sở thích
⭐ Tương tác thẳng hai phía nằm trong thầy cô
⭐ Học đến lớp lại cho tới lúc nào hiểu bài xích thì thôi
⭐ Rèn tips tricks chung bức tốc thời hạn thực hiện đề
⭐ Tặng full cỗ tư liệu độc quyền nhập quy trình học tập tập
Xem thêm: Axit oxalic - C2H2O4
Đăng ký học tập test không lấy phí ngay!!

Qua nội dung bài viết này, VUIHOC hy vọng rằng rất có thể chung những em nắm vững phần này kỹ năng về bảng tuần trả các nguyên tố chất hóa học. Để học tập nhiều hơn thế nữa những kỹ năng Hóa học tập 10 hao hao Hóa học tập trung học phổ thông thì những em hãy truy vấn fgate.com.vn hoặc ĐK khoá học tập với những thầy cô VUIHOC ngay lập tức lúc này nhé!