Bạn đang được bắt gặp trở ngại khi tham gia học cho tới số mol, độ đậm đặc mol, độ đậm đặc Tỷ Lệ vô môn Hóa Học trung học tập hạ tầng thì nội dung bài viết tiếp sau đây của công ty chúng tôi sẽ hỗ trợ chúng ta ôn tậm lại những công thức tính số mol, công thức tính độ đậm đặc mol và công thức tính độ đậm đặc phần trăm tương đối đầy đủ, cụ thể.
Số mol được kí hiệu là chữ n và nhằm tính được số mol những bạn cũng có thể vận dụng những công thức tính tiếp sau đây công ty chúng tôi share các bạn coi ngay lập tức.
Bạn đang xem: Công thức tính số mol, Nồng độ mol, Nồng độ phần trăm chính xác 100%
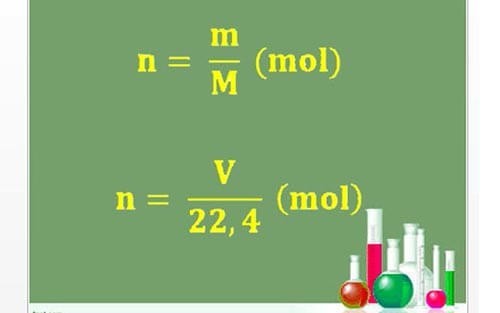
1. Cách tính số mol nguyên vẹn tử, phân tử theo đòi khối lượng
n = m/M
Trong bại :
- n là số mol hóa học (mol).
- M là lượng mol (g/mol): Là lượng mol của hóa học bại tính rời khỏi gam của N phân tử hoặc nguyên vẹn tử hóa học bại. Khối lượng mol có mức giá trị vì chưng phân tử khối hoặc phân tử khối của hóa học bại như lượng mol nguyên vẹn tử cacbon – C là 12 g/mol, lượng mol của phân tử amoniac – NH3 là 17 g/mol.
Các bạn phải lưu ý rằng, lượng mol của nguyên vẹn tử và phân tử là rất khác nhau. Ví dụ, lượng mol của phân tử Nito – N2 là 28 g/mol còn lượng mol của nguyên vẹn tử Nito – N là 14 g/mol - m là lượng của hóa học bại (g).
2. Cách tính số mol của hóa học khí ở ĐK chi tiêu chuẩn chỉnh (đktc)
n = V/22,4
Trong bại :
- n là số mol hóa học khí (mol).
- V là thể tích hóa học khí ở ĐK chi tiêu chuẩn chỉnh (lít).
- 22,4 là hằng số vô ĐK chi tiêu chuẩn chỉnh.
Đối với tình huống hóa học khí ở tình trạng bất ngờ, ĐK không giống với ĐK chi tiêu chuẩn chỉnh, các bạn ko thể dùng công thức bên trên nhưng mà nên cần thiết cho tới những công thức và phép tắc tính phức tạp rộng lớn.
Công thức tính độ đậm đặc mol
CM = n/V
Trong bại :
- CM Nồng phỏng mol
- n số mol hóa học tan
- V thể tích dung dịch
Lý giải: Nồng phỏng mol ngay số mol hóa học tan phân chia mang đến thể tích hỗn hợp.
Công thức tính độ đậm đặc phần trăm
C% = mct/mdd x 100%
Trong đó:
- C%: Nồng phỏng phần trăm
- mct: Khối lượng hóa học tan
- mdd: Khối lượng dung dịch
Mặt khác: mdd = mct + mdm (mdm là lượng của dung môi)
Lý giải : Nồng phỏng Tỷ Lệ vì chưng lượng hóa học tan phân chia mang đến lượng hỗn hợp và nhân với cùng 1 trăm Tỷ Lệ.
Bài tập dượt về công thức tính số mol, độ đậm đặc mol và độ đậm đặc Tỷ Lệ với đáp án
Bài tập dượt 1: Cho 14,4 lít nước hãy tính độ đậm đặc mol của hỗn hợp Khi hòa tan không còn trọn vẹn 31,6g KMnO4 vô đó
Lời giải:
Ta với số mol của KMnO4 là:
nKMnO4 = 31,6/15,8=0,2 (mol)
Nồng phỏng mol của hỗn hợp được xem là : Cm=0,2/31,6=0,0139
Bài tập dượt 2: Tính độ đậm đặc mol của hỗn hợp Khi hòa tan 32 gam NaOH vô vào 400ml nước. Giải mến.
Lời giải :
Đổi: 400ml =0,4 lít
nNaOH = 32/80= 0,4 mol
Áp dụng công thức tính độ đậm đặc mol:
C%= ( CMxM)/(10xD)
Xem thêm: Xe đạp điện 5 triệu | 8 mẫu hot nhất thị trường 2023
Trong đó:
CM=n
V=0,8:0,4= 2M
Tính độ đậm đặc mol của 5 lít hỗn hợp với chứa chấp 0,5 mol NaCl.
Lời giải:
Nồng phỏng mol sẽ tiến hành tính như sau:
CM = 0,5/5 = 0,1M
Bài tập dượt 3 : Tính độ đậm đặc mol của hỗn hợp Khi hòa tan 15,8g KMnO4 vô 5 lít nước.
Lời giải:
Số mol của KMnO4 là: nKMnO4 = 15,8/158 =0,1 (mol)
Nồng phỏng mol của dung dịch: CM = 0,1/5 =0,02M
Bài tập dượt 4: Trong 100ml hỗn hợp với hòa tan 8 gam NaOH. Tính độ đậm đặc mol của hỗn hợp.
Lời giải :
Ta với V = 100ml = 0,1 lít
nNaOH = 8/40 = 0,2 mol
Áp dụng công thức bên trên tao có:
CM = n/V =0,2/0,1= 2M
Bài tập dượt 5: Hòa tan không còn trăng tròn gam NaCl vô vào 40 gam nước. Hãy tính độ đậm đặc Tỷ Lệ của hỗn hợp này.
Lời giải:
Ta với lượng hỗn hợp là: mdd = mct + mdm = trăng tròn + 40 = 60 gam
Vậy độ đậm đặc Tỷ Lệ hỗn hợp là: C%= x 100% = x 100%= 33,3 %.
Kết luận: Vậy độ đậm đặc hỗn hợp của NaCl là 33,3%.
Bài tập dượt 6: Hoà tan 10 gam đàng vô 40 gam nước. Hãy tính độ đậm đặc Tỷ Lệ của hỗn hợp chiếm được.
Lời giải:
Ta với lượng hỗn hợp là: mdd = mct + mdm = 10 + 40 = 50 gam
Xem thêm: Cách pha màu nâu chuẩn tone, Cách phối màu ra màu nâu
Vậy độ đậm đặc Tỷ Lệ hỗn hợp là: C%= x 100% = x 100%= trăng tròn %.
Kết luận: Vậy độ đậm đặc hỗn hợp của đàng là 20%
Sau Khi phát âm kết thúc nội dung bài viết của công ty chúng tôi rất có thể hùn chúng ta lưu giữ được công thức tính số mol, độ đậm đặc mol và độ đậm đặc Tỷ Lệ nhằm áp dụng vô thực hiện bài bác tập dượt đúng đắn nhé












Bình luận